Som følge af hestepopulationens stigende alder bliver tumordiagnostik stadig vigtigere inden for hestepraksis. Laboratorietests bliver mere almindelige, som anvendelige og oftest non-invasive værktøjer for diagnose, prognose og som terapikontrol.
Tumordiagnostik er en af de største diagnostiske udfordringer for hestedyrlægen, på trods af stadig bedre billeddiagnostik og øget faglig viden.
De ofte uspecifikke symptomer, som feber, anoreksi, ødemer, vægttab samt adfærdsændringer kan skyldes en række sygdomme. Her kan laboratoriediagnostik give vigtig information og være en hjælp til diagnostikken.
Diagnostik ved levertumor
Alfa-1-fetoprotein
Hvis mistanke om levertumor (for eksempel hepatocellulært karcinom) kan alfa-1-fetoprotein (AFP) bestemmes. AFP er et glukoprotein, der dannes fysiologisk hos det perinatale føl (og indtil halvanden års alderen), og er derfor også fysiologisk forhøjet hos drægtige hopper. Hos voksne og ikke-drægtige heste kan en forøgelse være indikation på en levertumor: AFP dannes af de tumorlignende leverceller og findes derfor i forøgede koncentrationer i serum.
Alkalisk fosfatase (AP)
AP er mindre sensitiv ved diagnostik af levertumorer. Forøgede værdier ses hyppigere ved knoglemarvstumorer (for eksempel osteosarkom), som dog er yderst sjældne hos hest.
Diagnostik ved granulosacelle tumor (GCT)
Anti-Müllersk hormon (AMH)
Granulosacelle tumor er en af de hyppigste tumorformer hos hopper. Diagnosen kan oftest entydigt stilles vha. AMH-testen.
AMH er et glukoprotein, der påvirker den embryonale kønsdifferentiering, og hos de kønsmodne hopper dannes i granulosacellerne i follikulogenesen og hos hingste i sertolicellerne i testes. Derfor kan AMH-testen også benyttes til diagnostik af mange andre problemstillinger, foruden tumordiagnostik:
For diagnostik af granulosacelle tumor er AMH-testen, i forhold til både inhibin og testosteron, den mest sensitive testE.
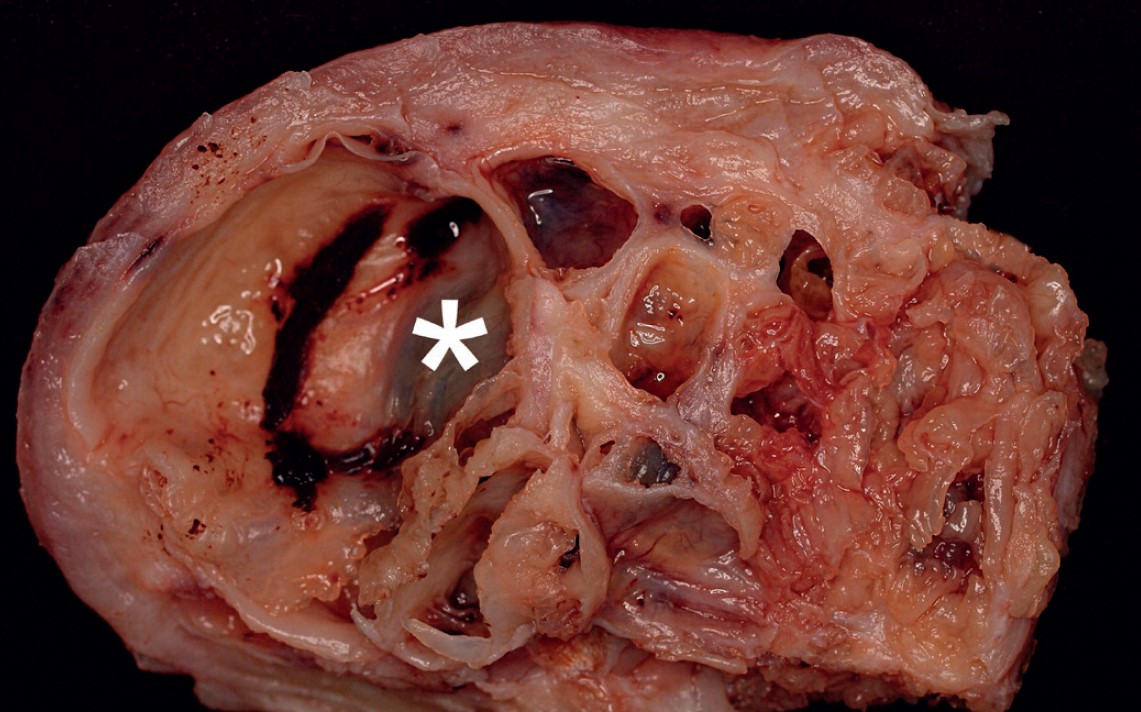
Klinisk udviser disse hopper typisk acykli med lave progesteronværdier (<1 ng/ml) og unilateralt forstørret ovarie med et helt karakteristik sonografisk udseende (Figur 1).
Det kontralaterale ovarie er oftest kraftigt formindsket i størrelse.
Differentialdiagnostisk er det ofte ikke muligt at stille diagnosen sonografisk ved andre ovariesygdomme, som ovarie-hæmatom, teratom eller cystadenom. Her kan AMH-testen hjælpe, da proteinet udelukkende dannes ved store mængder ensartede granulosaceller. Giver AMH-testen intet klart resultat, anbefales det at teste igen tre-fire måneder senere.
AMH kan også benyttes under drægtighed, da denne, modsat testosteron og inhibin, vedbliver at være konstant selv sidst i drægtigheden.
Under den normale cyklus udviser AMH ingen signifikante udsving og dannes udelukkende i ovariet, modsat testosteron, der også produceres i binyrebarken. Hos ældre hopper (>20 år) begynder AMH-værdien dog at synke i takt med follikelreserverne.
Også hos hingste finder AMH-testen anvendelse. Til kryptorkisme- diagnostik er AMH-testen også de tidligere anvendte østronsulfat og testosteron overlegne. AMH er her en meget nyttig, aldersuafhængig biomarkør for testikulært vævG. Basal testosteron kan ligge lavt, og endog under referenceværdien for kryptorkide hingste, og kan derfor ikke benyttes som diagnostisk test alene, men udelukkende som en hcG-stimulationstest, hvor både basal og stimulationsværdi måles.
På grund af AMH’s lange halveringstid (halvanden-to dage) bør man tidligst bestemme AMH to uger post kastration, hvor serumkoncentrationen er sunket så meget, så den er diagnostisk valid.
Inden for disse to uger kan man benytte hcG-stimulationstesten, skulle det blive nødvendigt, da testosteron har en kort halveringstid på blot cirka en time.
Meget lave AMH-værdier hos intakte hingste kan indikere te stikeldegeneration eller være sæsonbetinget (efterår/vinter). Testikeldegeneration hos ældre hingste ses ofte, men her kan en lav AMH intet sige om hingstens fertilitet.
Derimod kan meget høje AMH-koncentrationer, sammenholdt med kliniske symptomer, være en indikator på en sertolicelletumor og bør derfor altid undersøges nærmere histopatologisk.
Diagnostik ved lymfom
Equin lymfom er den hyppigst forekommende ondartede tumorform hos hest og inddeles i følgende former:
- Gastro-intestinal
- Kutan
- Mediastinal
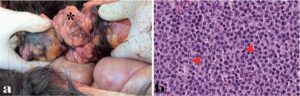
- Multicentrisk (Figur 2)
Prøveudtagning for en histopatologisk diagnose (gold standard) er, afhænging af placering og sygdomsstadie, ofte ikke mulig. Her finder tumorproliferationsmarkøren thymidin kinase anvendelseB.
Thymidin kinase
I veterinær smådyrspraksis samt humant benyttes thymidin kinase til diagnostik, terapikontrol samt evaluering af prognose. Det er et cellulært enzym, der spiller en afgørende rolle for DNA-syntesen, og derved celledelingen, når thymidin inkorporeres i DNA. Dets koncentration i serum stiger, når celledelingshastigheden stiger.
Eftersom maligne sygdomme i det hæmatopoietiske og lymfatiske system (lymfom, leukæmi, multipelt myelom) ofte er meget proliferative, kan thymidin kinase bestemmes som en såkaldt proliferationsmarkør.
Kraftige inflammationer kan dog også forårsage lavgradige stigninger i thymidin kinase, hvilket derfor må udelukkes som differential diagnose ved blandt andet at bestemme akut-fase-proteiner. Dog udelukker et negativt resultat ikke en underliggende tumorsygdom.
Atypiske lymfocytter
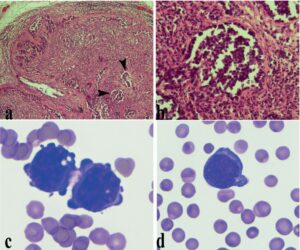
Ved lymfoproliferative neoplasier (Figur 4A og B) (lymfom stadie V, lymfatisk leukæmi) kan atypiske lymfocytter findes i det perifere blod. Oftest ses her leukocytose med lymfocytose eller neutrofili (ved myeloid leukæmi eller sekundær inflammation).
En cytologisk undersøgelse af lufttørrede, farvede blodudstrygninger vil allerede kunne give en indikation på et lymfom, såfremt denne diagnose mistænkes (Figur 4C og D), hvis der findes neoplastiske celler.
Punktater fra bughule eller thorax samt finnålsaspirater fra forstørrede lymfeknuder er også velegnede til cytologiske undersøgelse.
Flowcytometri
For at kunne klassificere i B- eller T-celle lymfom og for at skelne mellem lymfoproliferativ og myeloproliferativ leukæmi må flowcytometri benyttesC. Denne såkaldte immunofenotypning detekterer med hjælp fra bestemte antistoffer antigener på cellen, så celler kan klassificeres som T-hjælper, cytotoksiske T-celler og B-celler (Figur 3).
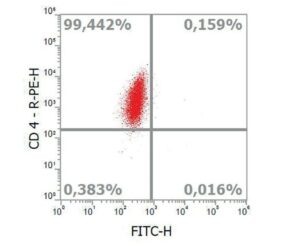
For flowcytometri kan følgende materiale anvendes:
- EDTA fuldblod
- Knoglemarv
- Punktat fra thorax og abdomen
- Finnålsaspirater fra lymfeknuder.
Når diagnosen lymfom er stillet histologisk, kan lymfomatypning ske ved hjælp af immunhistokemi.
Mistænkes lymfom bør der, foruden det store blodbillede, altid analyseres de klinisk kemiske parametre.
Heste med lymfom har ofte anæmi, trombocytopeni eller forhøjede akut-fase-proteiner (fibrinogen eller serum-amyloid A (SAA).
Yderligere laboratorie parametre
Akut-fase-proteiner
Akut-fase-proteiner, som serum-amyloid A (SAA) og fibrinogen, kan hjælpe med at estimere inflammationens sværhedsgrad samt vurdere resultat af terapienE.
Akut-fase-proteiner dannes som følge af en akut-fase-reaktion overfor en inflammation og er en uspecifik, systemisk reaktion på vævsskade forårsaget af infektion (bakteriel, viral eller parasitær), trauma eller neoplasi. Som følge af frigivelse af inflammationsmediatorer, som proinflammatoriske cytokiner, stimuleres leveren, foruden lokale og systemiske påvirkninger, til syntese af akut-fase-proteiner i hepatocytterne. En meget hurtig (6-12 timer) og kraftig stigning (100-1000-fold) ses ved påvirkning, og et lige så hurtigt fald (indenfor 12 timer) ses ved eliminering af skaden.
SAA er en yderst sensitiv markør for tidlig inflammation, der kan yde en vigtig hjælp for diagnose, prognose og monitorering.
Fibrinogen stiger noget langsommere (indenfor 24 timer) og ikke nær så kraftigt (1-2-fold) og når sin maksimale koncentration efter cirka 48 timer. Derudover kan den forblive høj op til et par uger, så den er derfor ikke så sensitiv som terapikontrol.
Serum-protein elektroforese
En yderligere, og meget billig, diagnostisk mulighed ved mistanke om tumor forekomst er også serum-protein elektroforesen. Monoklonale forandringer, ofte i beta- eller gammafraktionen, skyldes en overdreven produktion af et specielt immunglobulin sfa. en plasmacelle-klon og er hovedsageligt beskrevet ved lymfoproliferative sygdomme (Figur 5).
Paraneoplastiske forandringer, såsom hypercalcæmi, kan også give yderligere diagnostisk indsigtH.
Konklusion
Laboratoriediagnostisk er der flere forskellige, sensitive biomarkører til rådighed, som alene eller i kombination kan anvendes til diagnosestilling, vurdering af prognose, som terapikontrol eller hjælpe til behandlingsbeslutning.