Parkinson og Alzheimer rammer millioner af mennesker, men effektiv behandling mangler stadig. Dyremodeller – kemiske såvel som genetiske – er forskernes vigtigste redskab i jagten på svar.
Af specialdyrlæge, ph.d. & dr.med.vet. Aage Kristian Olsen Alstrup, Aarhus Universitetshospital.
De to hyppigste neurodegenerative sygdomme hos mennesker, Parkinsons sygdom og Alzheimers sygdom, er i vækst i disse år – primært som følge af den stigende levealder. Parkinsons sygdom opstår oftest fra slutningen af 50’erne og herefter med stigende forekomst (omkring 3 procent ved 80-års alderen). For Alzheimers sygdom stiger forekomsten fra cirka 3 procent hos de 65-årige til 25 procent hos dem over 85 år. Mens Parkinsons sygdom er hyppigst for mænd, er risikoen for Alzheimers sygdom størst for kvinder.
Ny serie om dyremodeller for menneskets sygdomme
DYRLÆGEN indleder med dette nummer en artikelserie om dyremodeller for menneskets sygdomme, og om, hvordan forsøgsdyr spiller en vigtig rolle for den biomedicinske forskning.
I næste nummer vil artiklen handle om dyremodeller for iskæmisk hjertesygdom, en af de væsentligste årsager til dødsfald i den vestlige verden.
Parkinsons sygdom er kendetegnet ved bevægelsesforstyrrelser (tremor, rigiditet og bradykinesi), mens Alzheimers sygdom giver kognitive og hukommelsesmæssige forstyrrelser. For begge sygdomme kendes en vis genetisk disposition, idet familiære former udgør knap 10 procent af Parkinsonstilfældene og knap 3 procent af Alzheimertilfældene, mens hovedparten er uden kendt genetisk disposition hos begge typer patienter. I mange år var nedgangen i hjernens dopaminproduktion centralt i forståelsen af Parkinsons sygdom, men i dag ved vi, at sygdommen også rammer andre dele af hjernen og endog resten af kroppen. Histologisk findes karakteristiske inklusionslegemer intracellulært i hjernens celler, kaldet Lewylegemer.
Parkinsons sygdom opstår enten i hjernen, hvorfra den spreder sig til resten af kroppen (brain first), eller den opstår i tarmene og derfra senere spreder sig til hjernen (gut first) – spredningen sker via nerverne. Alzheimers sygdom er kendetegnet ved tiltagende atrofi af hjernevævet med forstørrede hjerneventrikler. Ekstracellulært findes beta-amyloide plaques og intra-cellulære tau-tangles i hjernens celler. Der findes desværre i dag ingen behandlinger, der kan stoppe eller helbrede disse to alvorlige sygdomme, højst afhjælpe symptomerne på Parkinsons sygdom og midlertidigt udskyde symptomernes på Alzheimers sygdom. Behandlingen af Parkinsons sygdom er dog i dag så god, at sygdommen snarere er en lidelse, man dør med, end en lidelse man dør af. Anderledes er det desværre for Alzheimers sygdom, der medfører døden indenfor nogle år på trods af behandling.
Dyremodeller for Parkinsons og Alzheimers sygdomme
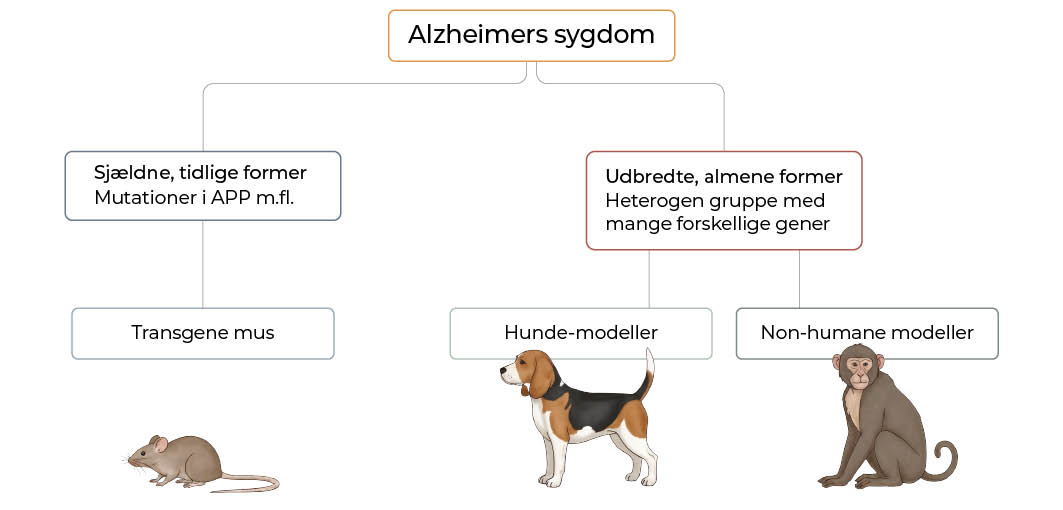
For både Parkinsons og Alzheimers sygdomme gælder, at sygdommene er forholdsvis specifikke for mennesker og det derfor er vanskeligt at gøre brug af spontane modeller hos forsøgsdyrene. Der findes dog en variant af Alzheimers sygdom hos hunde (Canine Cognitive Dysfunction), men selvom denne sygdom optræder spontant hos aldrende hunde af mellemstørrelse, og symptomerne minder en del om Alzheimers sygdom hos mennesker, så er patologien alligevel noget anderledes – blandt andet forankringernes placering i hjernen. I stedet anvendes i vid udstrækning genetiske og kemiske metoder til at inducere tilstandene. I det følgende gives en introduktion til nogle af disse modeller, idet der dog findes langt flere modeller end her beskrevet.
Kemiske modeller for Parkinsons sygdom
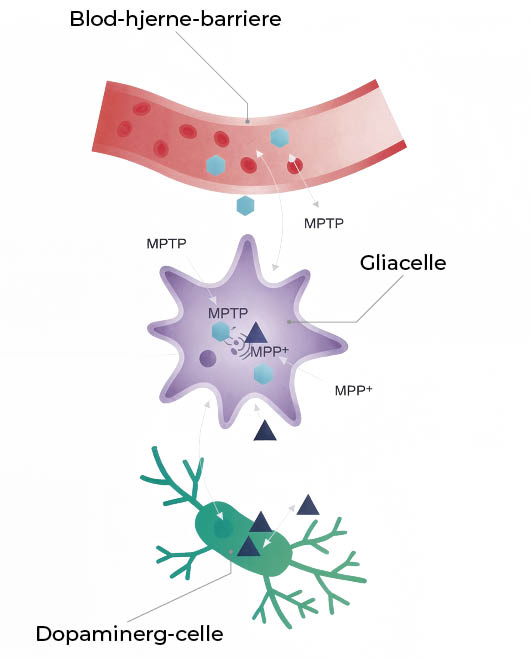
Traditionelt har en række kemiske forbindelse været anvendt til at skabe modeller for Parkinsons sygdom. Stofferne forårsager dopaminerg celledød, som det blandt andet er tilfældet med MPTP, der i hjernens støtteceller (gliaceller) omdannes til det toksiske MPP+ (figur 1). MPTP blev opdaget hos narkomaner, der havde indtaget dette giftstof, som ødelagde deres dopaminerge nervesystem.
Ved en nøje dosering er det muligt at reducere i antallet af dopaminproducerende celler, således at en vis parkinsonistisk tilstand opstår hos forsøgsdyr. Flere alternativer til MPTP anvendes også, blandt andet 6-OHDA, der stereotaktisk-kirurgisk deponeres lokalt i hjernens dopaminerge system. Denne model har den fordel, at den parkinsonistiske tilstand kan induceres unilateralt, hvorved forsøgsdyret har mulighed for at kompensere med den anden og raske side – dette vil i mange tilfælde forbedre dyrevelfærden ganske betragteligt. I de senere år er disse traditionelle modeller blevet suppleret med en række transgene dyremodeller, blandt andet en variant af SNCA-genet, der koder for alpha-synoclein-proteiner involveret i inklusionslegemerne.
Genetiske modeller for Alzheimers sygdom
Alzheimers sygdom har været forsøgt induceret i forsøgsdyr ad kemisk vej, men i dag dominerer de genetiske modeller. Der er således udviklet en lang række transgene musestammer, som alle er bærere af gener fra familier med tidligt indsættende Alzheimers sygdom. Mest kendt er den såkaldte svenske dobbeltmutation i APP-genet, som giver anledning til tidlig dannelse af beta-amyloid i hjernen. Musene overproducerer APP-genet og udvikler amyloid-plaques i hjernen inden cirka 1-års alderen. Tilsvarende findes knock-in modeller med andre gener, som også giver Alzheimerlignende sygdom, og det er muligt at kombinere flere muterede gener for at modulere både plaques og tau-tangles (figur 2). Gnaverforsøg suppleres ofte med forsøg på større forsøgsdyr, som hunde, grise og non-humane primater.

Testmetoder
Skanningsmetoder, såsom PET og MR, anvendes ofte, tillige med udpræget brug af postmortelle undersøgelser af hjernerne (histologi, autoradiografi mm). Med skanningerne er det muligt at undersøge både hjernens anatomi (struktur) og molekylære patologi i fortløbende serier, hvor sygdomsforløbet hos det enkelte forsøgsdyr kan følges. Det giver en bedre forståelse for sygdommenes udvikling hos det enkelte individ. Ved Alzheimers sygdom kan plaques monitoreres med PET-skanning, ligesom også stofskiftet i hjernen kan kortlægges. Også gangtest og adfærdstest anvendes ganske udpræget i dyremodellerne – for Alzheimers sygdom testes især den spatielle hukommelse i en række adfærdstest (figur 3).
Betydningen af aldrende forsøgsdyr
Der er et paradoks i, at selvom biomedicinsk forskning i overvejende grad omhandler sygdomme hos ældre mennesker, så er det oftest unge forsøgsdyr, der bliver anvendt til forskningen. Det er naturligvis i mange tilfælde problematisk.
Et eksempel var for testning af gut-first-hypotesen for Parkinsons sygdom. En række dyreforsøg udført på unge forsøgsdyr mislykkedes med at vise, at Parkinsons sygdom kunne startes op via tarmen.
Først da forsøgene i 2019 blev udført på aldrende mus og aldrende rotter lykkedes det at vise, at hypotesen er korrekt. Sidenhen er hypotesens rigtighed bekræftet i patienter med Parkinsons sygdom.
En sammenlignende oversigtsstudie har sidenhen dokumenteret, at dyreforsøg indenfor Parkinsons sygdom i højere grad giver pålidelige resultater, når man anvender aldrende forsøgsdyr.
For en række dyrearter, såsom grise, er det dog i dag slet ikke muligt at skaffe dyr der er tilstrækkelig gamle til at de har de aldersrelaterede svækkelser af hjerne og nervesystem.
Et nyt studie af grisehjerner, der er helt oppe på 8-11 år, har vist, at disse biologisk set snarere er midaldrende end gamle.
Dyrevelfærd
Forsøgsdyr med neurodegenerative lidelser kræver kærlig pleje og understøttende behandling. For Parkinsons sygdom er det oftest den nedsatte mobilitet, som der skal kompenseres for ved at sikre let adgang til vand og foder. Det er derfor også afgørende at observere, om dyrene i tilstrækkelig grad optager vand og foder. Det kan her være en fordel at anvende unilaterale modeller, som oftest med den raske side næsten fuld ud kan kompensere for den nedsatte dopamin-produktion. For Alzheimers sygdom skal det ligeledes sikres, at dyrene indtager væske og foder i tilstrækkeligt omfang, idet nedsat kognitiv funktion og hukommelsessvækkelse kan påvirke dyrenes evne hertil. Ligeledes skal der tages højde for, at dyrene ofte når at blive gamle i sådanne forsøg, og at andre aldersbetingede lidelser derfor kan opstå undervejs.