To af forskerne bag de såkaldte RNA-vacciner blev 10. december 2023 hædret med Nobelprisen i fysiologi eller medicin. Det var en forventelig pris, da vaccinerne viste sig egnede til bremsning af COVID19-pandemien.
Af Aage Kristian Olsen Alstrup, specialdyrlæge, ph.d. & dr.med.vet., Aarhus Universitet og Aarhus Universitetshospital.
Det forgange års videnskabelige gennembrud
Dynamitproducenten Alfred Nobel (1833-1896) ønskede i sit testamente, at nobelpriserne skulle gives til de forskere, der det forgangne år havde gjort de største videnskabelige gennembrud. Problemet med denne tilgang er dog, at man sjældent straks ved, om en ny opdagelse er vigtig eller ej; altså om resultaterne er langtidsholdbare.
Dette problem blev tydeliggjort, da den danske professor og rektor for Københavns Universitet, Johannes Fibiger (1867-1928) i 1927 fik tildelt Nobelprisen i fysiologi eller medicin for sin cancerforskning – blot seks uger før sin død. Det viste sig nemlig efterfølgende, at resultaterne slet ikke holdt vand. Denne og andre sager medvirkede til, at Nobel-komiteen i dag først uddeler nobelpriser mange år efter, opdagelserne er gjort. Dette er også tilfældet med Nobelprisen i fysiologi eller medicin i 2023, om end den konkrete anledning – COVID19-pandemien – var ret ny.
En forventelig nobelpris i 2023
I begyndelsen af oktober 2023 annoncerede det svenske Karolinska Instituttet, at forskerne Katalin Karikó (f. 1955) og Drew Weissman (f. 1959) var årets vindere af Nobelprisen i fysiologi eller medicin. Det var en helt forventelig nobelpris, da de to forskere står bag den nyeste teknologi, der blev anvendt til vaccination af verdens befolkninger mod COVID19.
Der er givet over 13 milliarder doser vacciner, og vaccinationsprogrammerne skønnes at have reddet millioner af menneskeliv og bremset COVID19-pandemien. Selvom COVID19-vaccinerne var nye, så havde teknologien bag mange år på bagen. Behovet for COVID19-vacciner havde blot været så presserende, at de sidste forhindringer på vejen nu var blevet ryddet af vejen.
RNA-vacciner er hurtige at udvikle og tilpasse
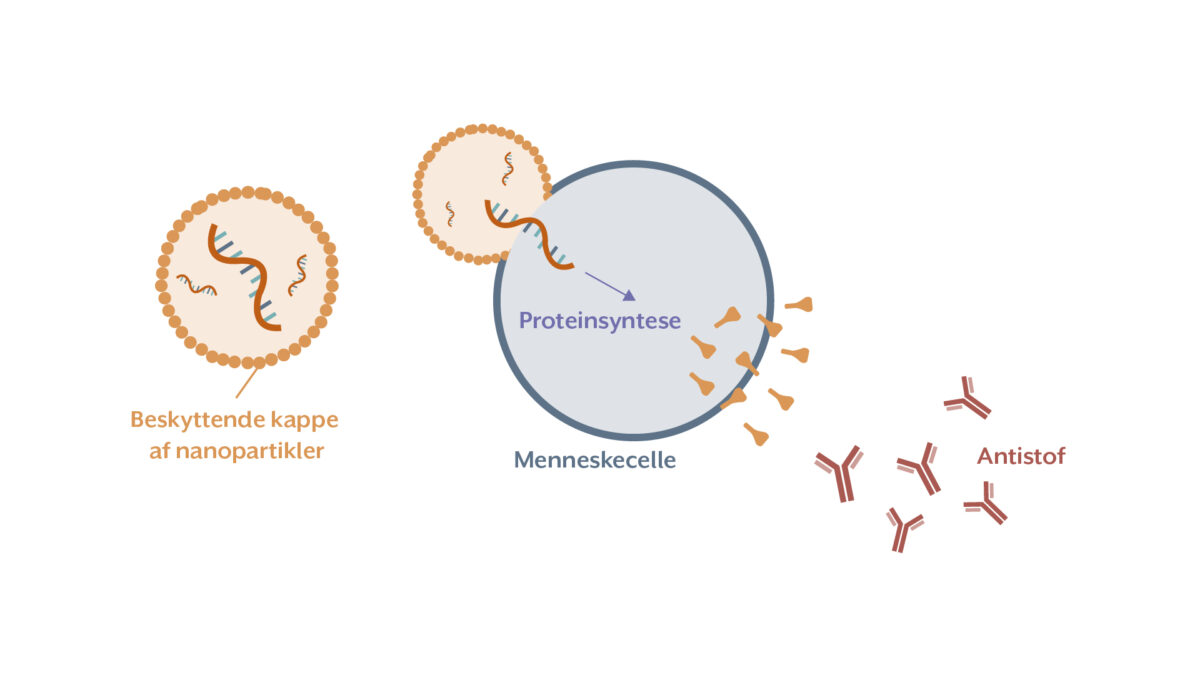
Ved traditionelle vacciner indsprøjtes hele eller dele af mikroorganismerne ind i kroppen, hvorefter immunforsvaret udvikler immunitet mod antigenerne. Ved RNA-vacciner indsprøjtes derimod den kodende RNA-streng (mRNA), hvorefter cellerne selv må producere antigenerne, som immunforsvaret efterfølgende reagerer mod.
Disse RNA-vacciner er relativt lette at producere, og det er også ret nemt og hurtigt at ændre på RNA-koderne, så de bliver tilpasset den aktuelle stamme af virus, som er i omløb. Det var Katalin Karikó og Drew Weissman tidligt opmærksomme på under COVID19-pandemien, og det lykkedes rekordhurtigt vaccineproducenterne at producere vaccinerne. Tidsperspektivet er selvsagt afgørende under pandemier.
Museforsøg førte til udvikling af RNA-vacciner
De første forsøg med såvel RNA- som DNA-vacciner foregik på mus i starten af 1990’erne.
I begyndelsen var forventningerne til DNA-vaccinerne størst, da DNA – som dobbeltstrenget molekyle – er mere stabilt end den enkeltstrengede RNA. Imidlertid viste det sig vanskeligt at overføre resultaterne med DNA-teknikkerne fra forsøgsdyr til mennesker.
Sandsynligvis var det vanskeligt at få DNA-molekylet helt ind i cellekernerne, hvor den kunne blive transskriberet, mens mRNA jo blot behøver nå ind i cytoplasmaet for at opnå translation. Selvom RNA-molekylet var relativt ustabilt, var der alligevel flest fremskridt at spore med denne. Et stort problem var dog, at syntetisk RNA lynhurtigt bliver nedbrudt i cellerne, ofte så hurtigt at proteinsyntesen ikke kan nå at producere tilstrækkeligt med antigen til at etablere en effektiv immunitet. Der var brug for et videnskabeligt gennembrud for at komme videre.
Gennembruddet kom i 2005
Den ungarskfødte biokemiker Katalin Karikó og den amerikanske læge Drew Weissman begyndte deres frugtbare samarbejde, da de en dag faldt i snak ved en kopimaskine på University of Pennsylvania. Katalin Karikós viden om biokemi kombineret med Drew Weissmans viden om immunforsvaret blev afgørende, idet de fandt frem til, hvordan syntetiske RNA-molekyler kan modificeres, så de ikke straks bliver nedbrudt i cellen. Dermed var der tid nok til, at proteinsyntesen kunne foregå i tilstrækkeligt omfang.
Denne vigtige opdagelse publicerede de i fællesskab i 2005, og dermed var en væsentlig forhindring for RNA-vaccinerne fjernet. Vi skal dog frem til december 2020 før RNA-vaccinerne – COVID19-vaccinerne fra Pfizer/BioNTechs og Moderna – var klar til klinisk brug i mennesker.
Rekorthurtig udvikling
11. januar 2020 offentliggjorde de kinesiske myndigheder gensekvensen for SARS-CoV-2 – altså det virus, der fører til COVID19. Og allerede 16. marts 2020 var MODERNA klar med en test-vaccine til den første testperson, 43-årige Jennifer Haller fra Seattle i USA. To måneder er rekordhurtigt for udviklingen af en ny vaccine.
RNA-vaccinen viste sig effektiv, blandt andet fordi antigenerne sandsynligvis produceres i større mængder og over længere tid end ved traditionelle vacciner. Dette giver immunforsvaret bedre mulighed for at udvikle effektiv immunitet ved RNA-vacciner, som i øvrigt giver både cellulær og humoral immunitet hos patienten. En ulempe ved RNA-vacciner er, at de kræver koldkæde-distribution før anvendelse. Dette på trods af at RNA-molekylet er pakket ind i en beskyttende kappe. RNA-vaccinerne er et vigtigt redskab at have ved hånden næste gang, der opstår en pandemi. COVID19 var den første pandemi, som det rent faktisk lykkedes at bremse ned med vacciner.
Dansker nomineret til nobelpris
Blandt årets øvrige nominerede forskere til Nobelprisen i fysi-ologi eller medicin var også den danske professor Jens Juul Holst (f. 1945) fra Københavns Universitet. Tilbage i 1986 opdagede han i grise tarmhormonet GLP-1, som er grundlaget for den medicin mod diabetes og fedme, som Novo Nordisk – med We-govy – er storsælgere af i øjeblikket. Da vi jo står i en fedmepandemi i øjeblikket, bliver det spændende at se, om opdagelsen af GLP-1 også en dag vil udløse en nobelpris.